РАЗДЕЛ 2. ЭНДОКРИНОЛОГИЯ
ГЛАВА 320. НАЧАЛА ЭНДОКРИНОЛОГИИ
Джин Д. Вилсон (JeanD. Wilson)
Функциональные свойства клеток определяются генетическими факторами, но скорость метаболических реакций в клетке регулируется в главном двумя взаимосвязанными и взаимодействующими системами —эндокринной и сердитой. Вначале эти две системы рассматривали как отдельные, в зависимости от способа передачи информации — с подмогою сердитых импульсов или химических передатчиков, поступающих в кровь. В истинное время стало светло, что такое представление недостаточно полно. Дело не только в том, что нейромедиаторы, например норадреналин, могут циркулировать в крови как гормоны, но и в том, что сердитые импульсы оказывают сильное воздействие на секрецию химических посредников, таких как тестостерон и инсулин. Это узкое взаимодействие необыкновенно явно в гипоталамусе, который является высшим интегративным центром обеих систем. Следовательно, интеграцию и координацию метаболических процессов в организме исполняет единичная нейроэндокринная система. Эндокринология занимается в главном химическими медиаторами в этой системе, но правильное понимание роли гормонов требует знания как автономной сердитой системы (см. гл.66), так и протекающих в клетке метаболических процессов.
В понятии эндокринология имеется и некоторая неопределенность. Термином «гормои» исходно означали вещества, секретирующиеся в кровь и действующие на ткани как химические эффекторы. Однако продуцировать такие химические медиаторы могут не только так нарекаемые эндокринные органы. Например, такие гормоны, как ангиотензины II и III, образуются в самой крови, а тестостерон у женщин и дигидротестостерон и эстрадиол у мужчин частично секретируются, а частично образуются в периферических тканях из циркулирующих в крови предшественников (так нарекаемых прогормонов). Отдельные химические медиаторы циркулируют лишь в ограниченных пространствах внеклеточной жидкости (например, в гипоталамо-гипофизарной портальной системе) и не попадают в существенных количествах в системный кровоток. Наконец, такие гормоны, как инсулин, дигидротестостерон и тиреотропин-рилизинг гормон (ТРГ), владеют паракринными эффектами в тех же тканях, в которых они образуются, а в отдаленных местах оказывают иное деяние. Поэтому при решении вопроса, является ли данный эффектор гормоном, необходимо учитывать как его деяние, так и происхождение.
Биохимия. Синтез.В истинное время у млекопитающих знаменито более 60 гормонов. Они делятся на три группы — пептиды или производные пептидов, стероиды и амины и синтезируются одним из двух путей. Если происходит синтез пептидных гормонов, гены кодируют информационную РНК, которая затем транслируется в белковые предшественники. Эти белки подвергаются посттрансляционному расщеплению (препропаратиреоидный гормон ®пропаратиреоидный гормон ®паратиреоидный гормон и проинсулин ® инсулин) и/или процессингу (тиреоглобулин ®тироксин ®трийодтиронин), в результате чего образуется активный гормон, распознаваемый тканью-мишенью. В синтезе пептидных гормонов отличительно то, что аминокислотную последовательность пептидов кодируют одни гены, а за превращение пептида в его окончательную форму ответственны иные. В пептидных гормонах, состоящих из субъединиц, различные субъединицы могут происходить либо из одного (инсулин), либо из различных предшественников [лютеинизирующий гормон (ЛГ)]. Больше того, один и тот же пептидный гормон (соматостатин) может образовываться из различных прогормонов, кодируемых различными генами, а отдельные прогормоны, такие как проопиомеланокортин, могут метаболизироваться различными клетками в различные гормоны в зависимости от комплекта ферментов процессинга, присутствующего в данной клетке (см. гл.69). Пептидные гормоны могут образовываться также эктопически при злокачественном перерождении неэндокринных органов, например, в раковой ткани легких (см. гл.303).
При синтезе стероидных гормонов окончательные продукты образуются в результате ферментативных превращений главного предшественника — холестерина (для большинства стероидных гормонов) или 7-дегидрохолестерина (для метаболитов витамина D). В превращении холестерина в эстрадиол участвуют не менее шести ферментов (или ферментных комплексов) и, следовательно, не менее шести различных генов. Из-за множественности необходимых ферментов синтез стероидов из холестерина раковыми клетками неэндокринных тканей маловероятен. Многие тканн, однако, неспособные образовывать стероидные гормоны из холестерина denovo, содержат ферменты, превращающие циркулирующие в крови стероиды в иные гормоны,как это происходит, например, при превращении андрогенов в эстрогены в опухолях трофобласта или прогестерона в дезоксикортикостерон в почках.
Гормоны, относящиеся к группе аминов, синтезируются в процессе реакций, аналогичных таковым при синтезе стероидных гормонов, за тем исключением, что предшественникам в данном случае служат аминокислоты. Например, предшественником адреналина и норадреналина является тирозин (см. гл.66).
Запасание.Большинство тканей, синтезирующих гормоны, не владеет способностью запасать готовый продукт в достаточном количестве. Например, в тестикулах взрослого человека содержится лишь около 1/6 распадающегося в сутки количества тестостерона, и поэтому для обеспечения нормальной суточной секреции этого гормона его тестикулярный пул обязан обновляться несколько раз в сутки. Даже в тех клетках, в которых имеются специальные органеллы для накопления гормона, запасаемое количество его обычно малюсенько: инсулиновые гранулы в панкреатических бета-клетках содержат такое количество инсулина, которого хватает лишь на краткое время, тогда как сердитые окончания имеют запас норадреналина на несколько дней. Ограниченная способность некоторых тканей накапливать гормоны обусловлена тем, что заключительные не могут химически включаться ни в одну из трех главных форм запасаемых веществ (липиды, гликоген или белок). Например, большинство стероидных гормонов слишком полярны, чтобы в веских количествах откладываться в липидах, а пептидные гормоны и амины не входят в состав белков. Поэтому содержание большинства гормонов в организме обычно малюсенько. Исключением являются те случаи, когда в белках или нейтральных липидах гормоны запасаются в виде предшественников: щитовидная железа содержит белок тиреоглобулин в количестве, достаточном для 2-недельной нормальной секреции тиреоидных гормонов, а предшественник и промежуточные формы витамина D могут в веских количествах кумулироваться в липидах печени.
Секреция
Биохимические механизмы, принимающие участие в секреторном процессе, исследованы не полностью. Полагают, что в одних случаях происходит превращение нерастворимых веществ в их растворимые производные (протеолиз тиреоглобулина с образованием тиреоидных гормонов); в иных секреция обусловлена экзоцитозом запасных гранул (инсулин, глюкагон, пролактин, гормон роста). Наконец, секреция может отражать пассивную диффузию свежесинтезируемых молекул, например стероидных гормонов, по градиенту концентрации в плазму; в этих условиях скорость секреции гормона могла бы отчасти определяться скоростью кровотока в ткани.
Из-за ограниченной способности к накапливанию большинство гормонов секретируется в плазму с той же скоростью, с какой образуется. Тропные гормоны гипофиза [ЛГ, адренокортикотропин (АКТГ), тиреотропин (ТТГ)] действуют на свои ткани-мишени, стимулируя одновременно и синтез, и секрецию гормонов этими тканями. Даже когда пептидные гормоны хранятся в гранулах, первоначальная секреция их сопровождается повышением скорости синтеза этих гормонов (например, при двухфазной секреции инсулина, вызываемой введением глюкозы). Секреция некоторых гормонов зависит от медли суток, сна или бодрствования, возраста и эмоционального состояния. Предполагают, что достаточно часто наблюдается сопряжение между синтезом и секрецией.
Быстрая регуляция секреции многих гормонов выучена плохо. Некоторые гормоны секретируются импульсно, т. е. в виде повторяющихся выбросов. Зависит ли такая интермиттирующая секреция от изменений скоростей синтеза, кровотока или каких-то иных механизмов, неведомо. Желая физиологическое значение пульсирующей секреции не до конца светло, изменение частоты или амплитуды гормональных выбросов в великой степени сказывается на эффектах гормонов. Так, импульсное введение рилизинг-гормона лютеинизирующего гормона (ЛГРГ) стимулирует секрецию ЛГ гипофизом, а введение тех же количеств ЛГРГ с постоянной скоростью (в течение определенного медли) оказывает противоположный эффект. Больше того, изменение частоты или амплитуды гормональных выбросов может описывать определенные патологические состояния. Так, нарушение суточного ритма секреции кортизола отличительно для ранней стадии хвори Кушинга.
Транспорт.Из мест синтеза к местам клеточного деяния, метаболической инактивации и распада гормоны поступают с лимфой, кровью и внеклеточной жидкостью. Для большинства пептидных гормонов и аминов плазма, вероятно, является пассивным растворителем, а для стероидных и тиреоидных гормонов она служит источником специфических связывающих эти гормоны транспортных белков. Таким образом, чем менее гормон растворим в воде, тем более главна роль транспортных белков. Ни один из знаменитых на сегодня транспортных белков не владеет в этом отношении исключительностью. Например, тестостерон может транспортироваться не только специфическим связывающим белком [тестостерон-эстрадполсвязывающий глобулин (ТЭСГ)], но и альбумином; тироксин транспортируется как преальбумином, так и тироксинсвязывающим глобулином (ТСГ). Гормон, связанный с белком (Г•Б), не может проникнуть в большинство внутриклеточных пространств и служит резервуаром, из которого свободный гормон (Г) маршрутом диффузии поступает внутрь клетки: Г+Б ÛГ•Б.
Соотношение связанного и свободного гормона в плазме зависит от количества гормона, количества связывающего белка и сродства белка к гормону. Однако эффективный уровень свободного гормона в организме зависит и от иных факторов. Например, при высокой скорости диссоциации гормона из комплекса со связывающим белком (большей, чем скорость капиллярного кровотока в данном органе) на свободную (функционально активную) фракцию гормона влияют как скорость капиллярного кровотока, гак и проницаемость мембран.
Для оценки эндокринной функции великое значение имеет понимание отношений между свободным и связанным гормоном. Во-первых, свободной (диализуемой) фракции гормона invitroобычно меньше, чем свободной фракции, существующей invivo. Это объясняется тем, что часть гормона, находящаяся в комплексе со слабо связывающими его белками, такими как альбумин (в противовес той части, которая находится в комплексе со специфическими связывающими белками, владеющими высоким сродством к гормону), живо отсоединяется от альбумина по мере того, как свободная фракция диффундирует из капилляров в ткани. Следовательно, гормон, связанный с альбумином invivo. может функционировать как свободная фракция. При многих состояниях величина диализуемой фракции служит надежным показателем кажущейся свободной фракции invivo. Однако в условиях гипоальбуминемии содержание свободной (диализуемой) фракции invitroможет увеличиваться, тогда как invivoуровень свободного гормона снижается. Кроме того, в тех тканях, например, в печени, где белки (в том числе и комплексы гормонов с транспортными белками) подвергаются разрушению (в отличие от иных тканей, где в клетки проникает только свободный гормон), количество поступающего в ткань гормона в меньшей ступени зависит от величины свободной фракции последнего.
Во-вторых, распределение гормонов между плазмой и тканью зависит от соотношения тканевых и плазматических связывающих белков. Поэтому правильные или кажущиеся уровни свободного гормона не отражают количество гормона в клетках.
В-третьих, только свободный гормон взаимодействует с периферическими клетками и участвует в регуляторных механизмах образной связи, контролирующих скорость гормонального синтеза. Вследствие этого изменения количества транспортного белка в равновесных условиях не могут вызывать эндокринной патологии, если, окончательно, не нарушены остальные звенья обратной связи в эндокринной системе. Например, резкое повышение или понижение уровня ТСГ (в силу генетических пли иных факторов) вовсе не непременно будет сопровождаться изменением тиреоидного статуса. Так, внезапное увеличение уровня ТСГ приведет к снижению содержания свободного (диализуемого) и связанного с альбумином гормона; это обязано обусловить повышение секреции ТТГ и продукции тироксина щитовидной железой, которая будет нарастать до тех пор, пока ТСГ снова не окажется насыщенным, а уровень свободного гормона возвратится к норме, что в свою очередь нормализует уровень ТТГ и секрецию тиреоидных гормонов. В обратной ситуации снижение количества ТСГ временно повысит содержание свободного гормона, а секреция ТТГ и тироксина будет снижаться до тех пор, пока этот уровень не возвратится к норме. Таким образом, можно сказать, что при изменении количества специфического белка, связывающего гормон с высоким сродством, может резко измениться уровень гормона, но само по себе это не может вызвать долгих симптомов излишка или недостаточности гормона, если только не нарушены регуляторные механизмы обратной связи, контролирующие синтез гормона. Однако в тех случаях, когда образование гормона не регулируется обычными механизмами обратной связи, изменение количества связывающего белка может послужить причиной эндокринной патологии. Например, у женщин уровень тестостерона непосредственно не регулирует его продукцию, и поэтому изменение количества ТЭСГ может обусловить хроническое изменение уровня свободного тестостерона.
Распад и кругооборот.Уровень любого гормона в плазме (УП) зависит от двух факторов — скорости секреции (СС) гормона и скорости его метаболизма и экскреции, общо именуемой скоростью метаболического клиренса (СМК): УП=СС/СМК или
СС=СМК•УП.
Метаболический клиренс гормона исполняется рядом механизмов. Маленькое количество интактного гормона выводится из организма с мочой и желчью. В тканях-мишенях, тканях, не являющихся мишенями (такие как печень и почки) или в тканях обеих групп гормон разрушается и инактивируется. Достаточно часто метаболизм гормона облегчает его экскрецию, делая его способным растворяться в моче или желчи. Пептидные гормоны инактивируются, как верховодило, протеазами тканей-мишеней. Тиреоидные гормоны дейодируются, дезаминируются и деконъюгируют в главном в печени. Стероидные гормоны восстанавливаются, гидроксилируются и конъюгируют с остатками глюкуроновой и серной кислот. Иногда конъюгаты с желчными кислотами в желудочно-кишечном тракте гидролизуются и вновь всасываются в кровь. Механизмы разрушения различных гормонов имеют одну общую черту: катаболизм всех знаменитых на сегодня гормонов может протекать по альтернативным путям.
Из-за необыкновенностей регуляторного механизма обратной связи изменение скорости распада гормона само по себе не может служить причиной эндокринной патологии, если только не нарушена обратная связь, которая регулирует синтез этого гормона. Например, при тяжелых заболеваниях печени и при микседеме нарушается деградация глюкокортикоидов в печени; в результате кругооборот кортизола замедляется, но его уровень в плазме не увеличивается, так как секреция АКТГ оказывается заторможенной. Таким образом, нормальный уровень свободного гормона поддерживается в результате снижения скорости секреции кортизола. Обратная ситуация наблюдается при ускорении распада глюкокортикоидов (как при тиреотоксикозе); в такой ситуации нормальный уровень гормона обеспечивается возрастанием его секреции.
Хотя изменения скорости распада гормона сами по себе не приводят к его дефициту или излишку, они имеют великое значение для эндокринной фармакологии. Так, у больных с микседемой или патологией печени глюкокортикоиды даже в обычных порциях могут вызывать синдром Кушинга, поэтому их дозировку необходимо снижать. Против, при гипертиреозе дозы глюкокортикоидов следовало бы увеличивать. Кроме того, возникновение гипертиреоза у лиц с недостаточными запасами надпочечников могло бы (за счет ускорения катаболизма глюкокортикоидов) вызвать адреналовый криз. Таким образом, при нарушении или неимении нормальных сервомеханизмов, регулирующих синтез гормонов, изменение скорости их распада может либо утяжелять, либо вызывать эндокринную патологию.
Регуляция продукции гормонов.Выше отмечалось, что уровень гормонов у здорового человека колеблется в результате изменения скорости их продукции, а заключительная прямо или косвенно регулируется метаболической активностью самого гормона. Такая регуляция исполняется за счет существования ряда петель обратной связи (рис.320-1). В некоторых случаях необходимо, чтобы уровень гормона в крови был взыскательно постоянным. Поэтому обязаны существовать какие-то сенсорные механизмы, следящие либо за уровнем самого гормона, либо за состоянием регулируемых им функций, таких как осмоляльность плазмы, концентрация глюкозы в крови, уровень кальция в плазме или содержание натрия в организме. Например, гормоны (кортизол, тироксин, половые стероиды), выделяющиеся под воздействием гипофизарных тропных гормонов, оказывают обратное деяние на гипоталамо-гипофизарную систему, регулируя скорость собственной секреции. Сходственно этому, секреция паратиреоидного гормона и инсулина зависит от обратных сигналов со стороны соответственно уровня кальция в сыворотке и глюкозы в крови. Системы обратных связей обычно более трудны, чем описанная схема; иногда они включают ряд промежуточных звеньев. В тех случаях, когда в роли обратного сигнала выступает непосредственно сам гормон (как, например, при деянии тестостерона на гипофиз), его эффект обусловливается теми же клеточными механизмами, которые определяют его деяние и в иных тканях-мишенях.

Рис.320-1. Гипофизарная регуляция таких эндокринных органов, как надпочечники, щитовидная железа или гонады, по механизму обратной связи.
Обратная связь может быть как отрицательной, так и положительной. Образцом положительной обратной связи служит стимуляция секреции Л Г эстрадиолом перед овуляцией. На регуляторные механизмы положительной или отрицательной обратной связи или на их реактивность могут влиять факторы негормональной природы и наружной среды.
Характерная необыкновенность систем обратной связи — быстрота функционирования. Действительно, в ответ на меняющиеся метаболические потребности большинство таких связей срабатывает за несколько минут или часов, обеспечивая гомеостаз в тесных границах. Исключения связаны с регуляцией гаметогенеза в яичниках и семенниках (см. гл.330 и 331). В обоих случаях в деяние вступают трудные процессы дифференцировки. В состоянии равновесия эти системы функционируют так, что продукция сперматозоидов непрерывно остается условно стабильной, а овуляция протекает циклично. Однако для завершения сперматогенеза требуется примерно месяц, и поэтому изменения уровня ФСГ длинное время могут не сказываться на скорости продукции сперматозоидов.
Тот факт, что секреция гормонов находится под регуляторным контролем, имеет важное клиническое значение. Во-первых, оценить клиническое значение уровня гормона в плазме можно только с учетом состояния подходящих регуляторных факторов (рис. 320-2). Понять, о чем свидетельствует некоторое снижение уровня тестостерона, можно лишь при одновременном определении уровня ЛГ. Точно так же, интерпретировать те или иные уровни инсулина ч паратиреоидного гормона в плазме можно лишь при одновременном определении соответственно содержания глюкозы и кальция в плазме. Во-вторых, данные об одновременном повышении уровня гормональных пар (пара гормон — регуляторный фактор) при неимении признаков излишка гормона указывают на существование резистентности к заключительному. Например, одновременно повышенное содержание в плазме глюкозы и инсулина отличительно для инсулинорезистентности; одновременное повышение уровней ЛГ и тестостерона свидетельствует о резистентности к андрогенам и т. д. В-третьих, понимание механизмов регуляции секреции гормонов сочиняет основу различных динамических тестов на запасы и секрецию гормонов.
Механизмы деяния гормонов.Первый этап деяния гормонов содержится в их взаимодействии со специфическими макромолекулами клетки, так нарекаемыми гормональными рецепторами, расположенными либо на плазматической мембране клеточной поверхности, либо в цитоплазме.
Гормоны, рецепторы которых расположены на поверхности клеток.Гормоны первого типа связываются поверхностными рецепторами, расположенными на плазматической мембране (рис.320-3). Распознают три вида взаимодействия гормонов с плазматической мембраной. При взаимодействии первого вида (Г, на рис.320-3) гормонрецепторный комплекс, находящийся на поверхности клеток, вызывает образование так нарекаемого второго посредника — циклического аденозин-3,5-монофосфата (цАМФ), и последующие деяния гормона опосредуются цАМФ (подробнее см. гл.67). Этот механизм отличителен для некоторых белковых гормонов и биогенных аминов. При взаимодействии второго вида (Г, на рис.320-3) рецептор клеточной поверхности индуци

Рис.320-2. Связь между уровнем гормона железы-мишени и уровнем тропного гормона в норме и при патологических состояниях (например, между ТТГ и тиреоидными гормонами, АКТГ и кортизолом, ЛГ и тестостероном).
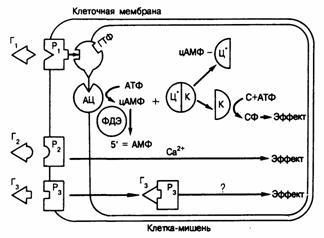
Рис.320-3. Схема деяния гормонов, рецепторы которых расположены на поверхности клетки.
Обозначения: Г— гормон, Р — рецептор, К — каталитическая субъединица протеинкиназы, Ц — цАМФ-связывающая субъединица протеинкиназы, цАМФ-циклический АМФ, АЦ— аденилатциклаза, С — субстрат, СФ — фосфорилированный субстрат, ФДЭ — фосфодиэстераза.
рует продукцию или высвобождение иных вторых посредников, например кальция. Этот механизм отличителен для некоторых нейротрансмиттеров и РТГ. Механизм высвобождения кальция и его деяния в такой системе неизвестен; вероятно, деяние кальция проявляется в его связывании с белком, регулирующим активность ферментов,— кальмодулином. При взаимодействии третьего вида (Г, на рис.320-3) комплекс поверхностный рецептор — гормон интернализуется внутрь клетки, но последующие события остаются неясными. К заключительней категории гормонов относится инсулин (см. гл.327).
Из этих систем лучше выучены те, в которых вторым посредником служит цАМФ (см. рис.320-3). Концентрация цАМФ в клетке регулируется двумя ферментами, обладающими противоположной активностью. Аденилатциклаза (АЦ), локализованная в плазматической мембране, превращает аденозинтрифосфат (АТФ) в цАМФ. Фосфодиэстераза (ФДЭ), находящаяся в главном в цитозоле клетки, инактивирует цАМФ, превращая его в 5-аденозинмонофосфат (5-АМФ). Гормоны (Г1), действующие на клеточную поверхность, образуют обратимые комплексы со специализированными белковыми рецепторами мембраны (Р1). Эти белки владеют высоким сродством к гормону, но имеют ограниченную емкость. Образование гормонрецепторного комплекса приводит к стимуляции аденилатциклазы. Комплекс Г1Р1 связывает N-субъединицу аденилатциклазы (которая связывает и ГТФ) и активирует каталитическую субъединицу АЦ, стимулируя тем самым синтез цАМФ. Фосфорилирующиеся ферменты, знаменитые под названием протеинкиназ, играют, по-видимому, ключевую роль в общем процессе. Эти киназы (ЦК) состоят из каталитических (К) и регуляторных (Ц) субъединиц. Связывание цАМФ с Ц высвобождает К, что приводит к фосфорилированию различных белков (С), сопровождающемуся их активацией или инактивацией.
Гормоны, рецепторы которых расположены внутри клетки. Стероидные и тиреоидные гормоны транспортируются в плазме, будучи связанными с белками-носителями (рис.320-4). Белково-связанные гормоны (ГБ) находятся в динамическом равновесии с маленькими количествами свободных гормонов (Г), которые пассивно диффундируют в клетки, где они действуют принципиально иным образом, чем пептидные гормоны. В большинстве случаев главная секретируемая в плазму форма гормона (кортизол, прогестерон, альдостерон, эстрадиол) не подвергается последующему метаболизму, и именно она обусловливает гормональный эффект в клетке-мишени. Иные гормоны (тироксин, тестостерон) подвергаются химическому превращению в более активные формы (трийодтиронин, дигидротестостерон).
Гормон связывается специфическим рецепорным белком(Р) цитоплазмы, образуя гормонрецепторный комплекс (ГР). Заключительный в ходе недостаточно выученного зависимого от температуры процесса подвергается трансформации, образуя активированный комплекс (ГР), способный связываться хроматином. В результате этого связывания образуются новые молекулы информационных РНК (мРНК) и усиливается синтез цитоплазматических белков. Заключительные в свою очередь опосредуют эффекты гормона. В некоторых случаях (трийодтиронин и отдельные стероиды) незанятые рецепторные белки локализуются преимущественно в ядрах; при этом свободный гормон проникает в ядро, где и образуется активный гормонрецепторный комплекс, подобным образом приобщающийся к хроматину.
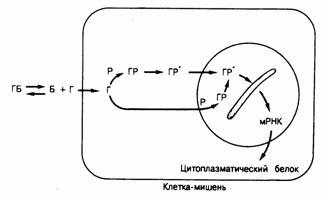
Рис.320-4. Механизм деяния гормонов, рецепторы которых расположены внутри клетки.
Обозначения: Г — гормон, Б — транспортныи белок плазмы, Р — рецептор. Р•—активированнып рецептор. мРНК — информационная (мессенджер) РНК.
Оценка гормональной функции.На практике эндокринный статус расценивают маршрутом определения уровней гормонов в плазме, экскреции гормонов или некоторых из метаболитов с мочой, скорости секреции гормонов, проведения динамических тестов на запасы и регуляцию гормонов, исследования гормональных рецепторов и отдельных эффектов гормонов в тканях-мишенях или с подмогою комбинации таких подходов. Каждая из этих методик оказывается полезной в конкретных клинических ситуациях.
Уровень гормона в плазме.Содержание стероидных и тиреоидных гормонов в плазме колеблется от 1 нМ до 1 мкМ, а пептидных гормонов — от 1 пМ до 0,1 нМ. Применение новейших химических, хроматографических, радиорецепторных и радиоиммунологических методик для определения веществ, присутствующих в плазме в низких концентрациях, появилось одним из крупных достижений современной медицины. Для оценки гормонального статуса в большинстве клинических ситуаций достаточно однократного определения содержания гормонов, уровень которых в плазме условно стабилен в различное время суток и в различные сутки (тироксин и трийодтиронин).
Однако по ряду причин к результатам таких определений следует относиться с осторожностью. Во-первых, химические и радиоиммунологические методы дозволяют получить правильное представление о содержании в плазме в данный момент только гормонов с условно простой структурой (стероидные и тиреоидные гормоны). У более трудных пептидных гормонов структуры физиологически активных гормональных молекул в плазме могут существенно варьировать, причем с подмогою специфических радиоиммунологических методик некоторые из них плохо поддаются определению. Например, стандартные радиоиммунологические методики определения ЛГ и паратиреоидного гормона могут подчас давать заниженные или завышенные результаты, описывающие количество биологически активного гормона в плазме. В таких ситуациях для оценки эндокринного статуса можно применять радиорецепторные или биологические методы определения гормонов invitro.
Во-вторых, при определении гормонов, секреция которых имеет пульсирующий характер (ЛГ, тестостерон), нельзя быть уверенным в том, что результат однократного определения отражает средний уровень гормона в плазме. В этих случаях определение нужно проводить либо в нескольких пробах плазмы, отбираемых случайным образом, либо в аликвотах объединенных трех — четырех проб плазмы, отбираемых с 20—30-минутными интервалами.
В-третьих, когда уровень гормона в плазме колеблется (например, суточные колебания концентрации кортизола), отбор проб плазмы можно приурочить к тому медли, которое дозволяет точнее судить о гормональном статусе. Однако и при этом следует помнить, что уровень гормона в плазме может колебаться в течение суток только в определенные периоды жизни (содержание ЛГ в ранние стадии пубертата). Правильная интерпретация содержания гонадотропинов, прогестерона и эстрадиола в плазме крови женщин детородного возраста требует учета фазы овуляторного и менструального циклов, и иногда, чтобы получить поддающиеся интерпретации данные, приходится последовательно проводить анализы в течение многих дней. Уровень некоторых гормонов (таких как тироксин и тестостерон) зависит и от сезонных колебаний, но они обычно столь малы, что не влияют на интерпретацию отдельных результатов. Иногда колебания уровня гормонов обусловлены не какой-то явной ритмичностью, а обострениями и затуханиями патологического процесса. Так, для диагностики синдрома Кушинга или гиперпаратиреоза могут потребоваться повторные определения содержания кортизола или кальция и паратиреоидного гормона в течение многих месяцев.
В-четвертых, если речь идет о стероидных и тиреоидных гормонах, которые присутствуют в плазме в главном в связанном с белками виде, определение общей концентрации их дает представление об эндокринном статусе только в той ступени, в какой оно позволяет судить об уровне свободного, или несвязанного, гормона. На самом деле содержание свободных гормонов (как верховодило,1% или меньше от общего их содержания) определяют лишь в немногих лабораториях. Так как количество свободного гормона зависит от количества и сродства связывающих транспортных белков и общего количества гормона, заключительное отражает уровень свободного гормона лишь постольку, поскольку количество связывающего белка (белков) остается постоянным или колеблется лишь в тесных пределах. При повышении содержания связывающего белка (ТСГ и ТЭСГ при беременности) или его снижении [потомственное снижение ТСГ и кортикостероидсвязывающего глобулина (КСГ)], чтобы судить об уровне свободного гормона, следует применять методы, позволяющие определять количества связывающего белка (поглощение Т, смолой для ТСГ или прямое определение ТСГ, ТЭСГ или КСГ).
В-пятых, концентрация большинства гормонов в плазме среди здорового народонаселенья колеблется в широких пределах. Следовательно, у какого-либо человека уровень гормона может снижаться или подрастать даже вдвое (и это будет резким нарушением для данного человека), но все еще оставаться в так нарекаемых нормальных пределах. Поэтому часто возникает необходимость одновременного определения уровня подходящих гормональных пар (ЛГ и тестостерон, тироксин и ТТГ). Уровень тестостерона на нижней границе нормы на фоне повышенного содержания ЛГ в плазме указывает на недостаточность семенников, тогда как тот же уровень тестостерона при нормальной концентрации ЛГ свидетельствует о нормальном эндокринном статусе (см. рис.320-2). Сходственно этому, у женщин с повышенной продукцией тестостерона и вторичным снижением уровня ТЭСГ концентрация тестостерона в плазме может быть нормальной, несмотря на нарушение его продукции.
Экскреция с мочой. Определение экскреции гормона или его метаболита с мочой, что отражает уровень данного гормона в плазме или скорость его секреции, владеет некоторыми превосходствами перед отдельным определением его уровня в плазме, так как дает представление о средней концентрации гормона в плазме за период сбора мочи. Действительно, уровень свободного кортизола в суточной моче может лучше отражать функцию кожуры надпочечников, чем результат однократного определения концентрации кортизола в плазме. Однако вновь-таки необходимо учитывать определенные ограничения такого подхода.1. Чтобы убедиться в правильности сбора мочи, всегда следует определять содержание в ней креатинина. Женщины экскретируют в сутки примерно
Скорости секреции и продукции.Определение реальной скорости секреции гормона дозволяет избежать многих мрачных моментов, возникающих при измерении уровня гормона в плазме и его экскреции с мочой. Методика таких измерений включает введение радиоактивного гормона и учет разведения, которому подвергается ловка вследствие смешивания с эндогенно секретируемым за определенное время нерадиоактивным гормоном. На практике выделяют из плазмы сам гормон, а из мочи — его специфический метаболит, очищают их до радиохимической гомогенности и полученный результат (в цифровом выражении) используют для расчета секретируемого за время исследования количества гормона. Если речь идет о гормонах, образующихся основным образом в периферических тканях (эстрадиол и дигидротестостерон у мужчин, трийодтиронин у мужчин и женщин), можно вводить меченые предшественники и для оценки общей скорости продукции измерять скорость их превращения в данные метаболиты. Вероятен и иной подход к определению скорости секреции. Для этого нужно знать скорость клиренса гормона и средний его уровень к плазме. К раскаянью, все эти методики трудны и трудоемки, требуют применения радиоактивных изотопов и могут выполняться лишь в немногих центрах.
Дииамические тесты на запасы гормонов и гормональную регуляцию. При выраженной гипо- или гиперфункции эндокринной железы для постановки диагноза достаточно определить уровень гормона в крови или моче, необыкновенно если тестирование обнаруживает сохранность обратных связей. Например, низкий уровень тестостерона в плазме па фоне высокого содерж