Данная информация предназначена для профессионалов в области здравоохранения и фармацевтики. Пациенты не обязаны использовать эту информацию в качестве медицинских советов или рекомендаций.
Использование самораскрывающихся металлических стентов для
лечения острого кровотечения из варикозно-расширенных вен пищевода
Дж. Бодладж(1)
М. Цомпо(2)
Л. Бенке(3)
П.Пичлер(4)
С.Аль-Хатиб(4)
Р.Киблбек(4)
А.Шамиех(5)
Дж.Биесенбах(1)
Учреждения
1. 2-я кафедра внутренних хворей больницы общего профиля г. Линц, Австрия
2. Институт патологии и микробиологии, клиника общего профиля г. Линц,
Австрия
3. Институт оперативной эндоскопии и лапароскопии Людвига Больцмана, клиника
общего профиля г. Линц, Австрия
4. Институт радиологии, клиника общего профиля г. Линц, Австрия
5. 2-я кафедра хирургии, Институт оперативной эндоскопии и лапароскопии
Людвига Больцмана, клиника общего профиля г. Линц, Австрия
Автор, водящий переписку:Р. Хубман, врач – 2-я кафедра
внутренних хворей. Allgemeines Krankenhaus der Stadt Linz. Krankenhausstrabe
9.4020Linz.Austria.
Библиография: Эндоскопия 2006; 38 (9): 896-901c Георг
Тиеме Ферлаг КГ Штутгарт-Нью-Йорк DO 10.1055/s-2006-944662 – ISSN 0013-726X
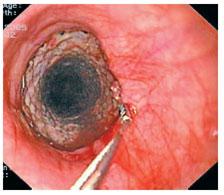
Предпосылки и цели исследования: Острое кровотечение из
варикозно-расширенных вен пищевода – это осложнение цирроза печени,
представляющее серьезную угрозу для жизни пациента. Существенно главными
факторами выживания после кровотечения из варикозно расширенных вен пищевода
являются быстрота и эффективность остановки кровотечения на начальном этапе.
Эндоскопическая и вазоактивная терапия являются золотым стандартом в лечении
острого кровотечения из варикозно-расширенных вен пищевода. Главная цель
данного исследования была оценить использование самораскрывающихся
металлических стентов для остановки некорригируемого острого кровотечения из
варикозно-расширенных вен пищевода.
Пациенты и методы: В период с ноября 2002 года и по май
2005 года пищеводные стенты были имплантированы 20 пациентам (18 мужчин, 2
женщины; средний возраст 52 года, в диапазоне от 27 до 87 лет) с массивным
продолжительным кровотечением из варикозно-расширенных вен пищевода как
альтернативное лечение к балонной тампонаде. Предшествующее консервативное или
эндоскопическое лечение было безуспешным. У пациентов отмечалось от 1 до 5
эпизодов кровотечения (в среднем 2,4). Восемь пациентов было с циррозом печени
ступени В по градации Чайлда-Пуга и 12 пациентов – со ступенью С. Был
разработан новый вид пищеводного стента со специальными вводящими
устройствами, которые обеспечивали имплантацию стента без применения
рентгенографического контроля.
Результаты: Стенты были удачно установлены у всех
пациентов и оставлены на 2-14 дней. Кровотечение из варикозно- расширенных вен
пищевода прекратилось сразу же после имплантации стента во всех случаях. Пока
стент находился на месте, предпринимались последующие диагностические деянья
по оптимизации лечения главного заболевания и портальной гипертензии. За
время лечения с использованием пищеводных стентов не отмечалось случаев
повторных кровотечений, болезненности или смертности. Все стенты были
извлечены безо всяких осложнений после начала лечения в соответствии с
конечным диагнозом.
Выводы: В этом экспериментальном исследовании был
предложен новый метод имплантации пищеводного стента как безопасное и
эффективное лечение массивного кровотечения из варикозно расширенных вен
пищевода у пациентов с циррозами печени. Эти первые клинические результаты,
окончательно, обязаны быть подтверждены в сравнительных исследованиях, включающих
великое количество пациентов.
Введение
Кровотечение из варикозно-расширенных вен пищевода – это самое строгое
осложнение портальной гипертензии. За заключительные 30 лет, 5-летний уровень
причинной смертности пациентов, госпитализированных с кровотечением из
варикозно расширенных вен пищевода, сократился с 49 до 31 % (1). Первый эпизод
кровотечения из варикозно расширенных вен пищевода кончается летальным
исходом в 30-50% случаев в течение 6 недель (2). Прыткая и эффективная
остановка кровотечения в самом начале играет основную роль в выживании больных.
Стандартная терапия включает: стабилизацию состояния пациента и проведение
профилактики антибиотиками; как можно быстрее до эндоскопической терапии обязана
быть начата вазоактивная терапия. Эндоскопическая терапия стала золотым
стандартом в лечении острых кровотеченией из варикозно расширенных вен
пищевода (3). В идеале, она обязана быть проведена в течение 6 часов после
поступления пациента в стационар (4).Такой вид лечения останавливает
кровотечение примерно в 90% случаев (3,5). В том случае, если
стандартная терапия слаба остановить острое кровотечение, показатель
смертности подрастает до 80%. Особой опасности подвергаются пациенты,
перенесшие несколько предшествующих оперативных вмешательств (6). В ситуациях,
когда стандартное лечение не подсобляет, показана балонная тампонада или
экстренная установка трансягулярного внутрипеченочного портокавального шунта
(7). Балонная тампонада широко доступна и легко применима в неотложных
случаях; однако, у нее также имеется ряд изъянов (8).
Покрытые оболочкой самораскрывающиеся металлические стенты (СРМС) являются
признанным средством в лечении новообразований пищевода (9). СРМС также могут
быть использованы для сдавления варикозно-расширенных вен пищевода. В том
случае, если не удается прытко остановить кровотечение маршрутом использования
стандартной фармакологической и эндоскопической терапии, то для этой цели мы
используем СРМС. Оценка эффективности имплантации СРМС в достижении гемостаза,
демонстрирующая безопасность метода и неименье осложнений от самой процедуры
и привела к творенью специального стента для использования необыкновенно у
пациентов с кровотечением из варикозно расширенных вен пищевода.
Пациенты и методы
С ноября 2002 по май 2005 в клинике общего профиля г. Линц было проведено
11 900 гастроскопий. За этот период всего было пролечено 143 пациента с
кровотечением из варикозно расширенных вен пищевода. В случае недоверия на
кровотечение из варикозно расширенных вен пищевода лечение начиналось с
вазоактивной терапии (соматостатин) и лечения антибиотиками (4). После
стабилизации гемодинамики, в течение 24 часов, по возможности в самые ранние
сроки проводилась эндоскопия. Попытка остановить кровотечение из варикозно
расширенных вен пищевода эндоскопическим методом предпринималась у каждого
пациента, и это было удачным у 128 пациентов (90% всех случаев).
Однако у 15 пациентов фармакологическая и эндоскопическая терапия не
обеспечила адекватного контроля кровотечения, и поэтому у них были введены
самораскрывающиеся металлические стенты вместо обычного применения балонной
тампонады. Кроме того, 5 пациентов с неуправляемым кровотечением из варикозно
расширенных вен пищевода были переведены из иных больниц; трех из них врачевали
с применением балонной тампонады зондами Сенгстакена-Блейкмора. После того,
как тампонада была прекращена и эндоскопически было диагностировано
длящееся кровотечение, безотлагательно был введен стент. Два иных пациента
были направлены бригадой наших эндоскопистов и для остановки кровотечения им
вместо балонной тампонады были имплантированы пищеводные стенты. В целом 20
пациентам (18 мужчин и 2 женщины) были установлены СРМС для остановки
кровотечения из варикозно расширенных вен пищевода.
Все 20 пациентов ранее перенесли несколько эпизодов кровотечения (от 1 до
5, в среднем 2,4) несмотря на предшествующие эндоскопические вмешательства.
Предшествующее лечение включало: наложение лигатуры, (количество=5; в среднем
от 1 до 5), склеротерапию (количество =5, четыре пациента после одной
процедуры и один – после двух процедур), и балонную тампонаду (количество =6;
варьирует от 1 до 3 раз). Средний возраст пациентов был 52 года (в возрасте от
27 до 87 лет). Кровотечение было вызвано циррозом печени алкогольного генеза
(11 случаев), иммунологическим или криптогенным циррозом (3 случая), либо
язвой желудка в комбинации с кровотечением из варикозно расширенных вен
пищевода. У 8 пациентов был цирроз ступени В по классификации Чайлда-Пуга и у
12 пациентов – цирроз ступени С (Табл. 1).Стенты были установлены с целью
лечения острого непрекращающегося кровотечения, как следует ниже. В случае
необходимости седативной терапии, в/в использовался мидазолам (постепенными
порциями по 2,5-10 мг), с флюмазенилом в качестве добавления для устранения
седативного деянья, вызванного бензодиазепином. Три СРМС стента были
установлены у интубированных больных; 17 пациентов поступили в эндоскопическое
отделение очень прытко, что позволило начать правильное лечение после первых
признаков кровотечения в течение 3 часов максимум.
Первые пять стентов были установлены с поддержкою проводникового катетера под
рентгенографическим контролем, что обеспечило правильную установку стента
через желудочно-пищеводный переход. Дважды были использованы стенты Чу
(диаметр 18мм, длина 140 мм) и три раза – стенты Элла-Бубелла-Дениша (диаметр
20 мм, длина 95 мм) (Табл.1).
Затем в нашей лаборатории был разработан новый вид стента, Элла-Дениша,
(диаметр 25 мм, длина 135 мм). Стенты Элла-Дениша были использованы у 15
следующих пациентов. Стенты Элла-Дениша были установлены с поддержкою специальных
интродьюсеров, которые дозволяют установку стента без рентгенографического или
даже эндоскопического контроля (Рис.1). Стент Элла-Дениша был установлен сразу
проксимальнее позиционного баллона с воронкообразного конца. Правильная
установка выполнялась маршрутом раздуванием баллона на дистальном конце вводящего
устройства для обеспечения правильного позиционирования, когда баллон
втягивался в кардию перед высвобождением стента. После расправления стент
сдавливал варикозно расширенные вены пищевода. Баллон сдувался и устройство
удалялось. После имплантации стента проводилась эзофагогастроско ия, и в
течение 12 часов проводилась рентгенография грудной клетки для того, чтобы
удостовериться в правильном расположении стента. Вазоактивная терапия
соматостатином прекращалась через 12 часов после установки стента. Снижение
геморрагии подтверждалось последующей гастроскопией.
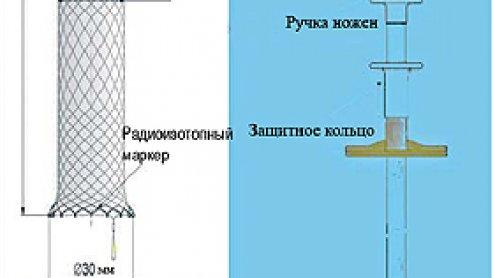
Рисунок 1. Конструкция стента SX-Элла-Дэниса
После стабилизации состояния верхняя часть тела пациента располагалась
слегка приподнято (под углом примерно 30 градусов), чтобы снизить риск
рефлюкса и аспирации. Жидкая еда и вода разрешались через 2 часа после
установки стента. На следующий день все, кроме трех пациентов с СРМС,
находящихся в коме, были в состоянии принимать жидкую или тщательно протертую
еду (чтобы не допустить смещения или окклюзии). При наличии симптомов
энцефалопатии, объем белка ограничивался. Для предотвращения и лечения
энцефалопатии, по необходимости применялся Л-орнитин-Л-аспартат, лактулоза и
неомицин.
У всех пациентов, кроме трех, находящихся в печеночной коме, было получено
информированное согласие. После того как всеми признанными методами остановить
кровотечение не удавалось, в качестве заключительного спасительного средства
использовался стент.
Таблица 1. Характеристика пациентов, лечение и исходы.
| Ф.И. | Воз- раст |
Этиология цирроза | Классификация по Чайлд-Пугу | Эпизоды предыдущих кровотечений | Предшествующее лечение кровотечений | Вид стента | Длительность нахождениястента (дни) | Окончательное лечение после стентирования | 30-дневное наблюдение | 60-дневное наблюдение |
| IR | 27 | Вирусный | С | 2 | 2хНЛ | а | 7 | Консервативное | Жив | Умер |
| NW | 36 | Алкогольный | В | 3 | 2хНЛ, 1хСТ | b | 5 | Невыполнение предписаний | Жив | Жив |
| HF | 56 | Криптогенный | С | 5* | 5хНЛ, 3хБТ | b | 6 | Азигопортальное разъединение и трансплантация | Жив | Жив |
| PM | 49 | Иммуно-логический | С | 1 | 1хНЛ | b | 5 | ТIPS и трансплантация | Жив | Жив |
| AK | 56 | Алкогольный | В | 2* | 1хНЛ.1хСТ, 1ХВТ |
с | 5 | Наложение лигатуры | Жив | Жив |
| SA | 36 | Алкогольный | В | 2 | 2хНЛ | а | 5 | Наложение лигатуры | Жив | Жив |
| KW | 44 | Криптогенный | В | 2* | 2хНЛ, 1хБТ | с | 5 | Азигопортальное разъединение | Жив | Жив |
| TD | 32 | Криптогенный | В | 1* | 1хНЛ | с | 3 | ТIPS | Жив | Жив |
| WG | 45 | Язва+ алкогольный |
С | 1 | 1хСТ | с | 1 | ТIPS | Жив | Жив |
| SR | 57 | Алкогольный | С | 3 | 2хНЛ.1хСТ, 1хБТ |
с | 7 | Азигопортальное разъединение | Жив | Жив |
| AH | 57 | Алкогольный | С | 3 | 2хНЛ.1хСТ | с | 7 | Азигопортальное разъединение | Жив | Жив |
| GJ | 69 | Алкогольный | В | 3 | 3хНЛ | с | 6 | Наложение лигатуры | Жив | Умер |
| KH | 63 | Алкогольный | С | 2 | 2хНЛ | с | 14 | Наложение лигатуры | Жив | Жив |
| ZD | 48 | Вирусный | С | 4 | 2хНЛ.2хСТ, 2хБТ |
с | 3 | Фатальный исход (печеночная недостаточность) | Умер | Умер |
| SE | 52 | Алкогольный | С | 1 | 1хНЛ | с | 9 | Хирургическая установка кольца под контролем рентгеногр. |
Жив | Жив |
| BD | 50 | Алкогольный | С | 3* | 3хНЛ,1хБТ | с | 10 | Азигопортальное разъединение | Жив | Жив |
| HH | 63 | Криптогенный | С | 2 | 2хНЛ | с | 5 | ТIPS | Жив | Жив |
| SA | 87 | Алкогольный | С | 1 | 1хНЛ | с | 5 | Фатальный исход (печеночная недостаточность) | Умер | Умер |
| NL | 38 | Алкогольный | В | 1 | 1хНЛ | с | 7 | ТIPS | Жив | Жив |
| HK | 52 | Вирусный | В | 1 | 1хНЛ | с | 2 | Наложение лигатуры и трансплантация | Жив | Жив |
* Переведенные из иных больниц,
НЛ- наложение лигатуры; БТ- балонная тампонада; СТ-склеротерапия
А. Стент Чу NES-18-080-070, М.АЙ.,Теч Co./Ltd; проводной шнур
В. Пищеводный стент Boubella с комплектом для введения; проводной шнур
С. Стент Дениша, набор с системой интродуктора; Елла-Дениша-Си-Эс; без
проводного шнура.
Смертность: 1-й- пациент бедность печеночной трансплантации; 12-й,
14-й и 18-й пациенты-печеночная недостаточность.
Результаты
Установка стента была удачной и прошла без осложнений у всех 20 пациентов,
кровотечение остановилось сразу же после его имплантации. У одного пациента
было кровотечение сразу из двух мест, пищеводное и желудочное. Желудочная
локализация была определена после остановки кровотечения из варикозно
расширенных вен пищевода имплантированным стентом. Данный пациент перенес
тотальную гастрэктомию и открытое портальное разъединение в качестве
конечного лечения.
У оставшихся 19 пациентов кровообращение стабилизировалось в течение 2
часов. Во время пищеводного стентирования не отмечалось ни случаев рецидива
кровотечений из пищевода или желудка, ни местных осложнений, таких как
усиление кровотечения, перфорация, или фистулизация, вызванных установкой
стентов. Смещение стента в желудок наблюдалась у 5 пациентов (один из двух
пациентов со стентами Чу, два из трех пациентов со стентами Boubella, и два из
15 пациентов со стентами Дениша). Смещение стента в желудок произошло из-за
очень низкого расположения стента. Смещение стента не сопровождалось повторным
кровотечением, и во всех этих случаях просто была проведена их репозиция с
поддержкою эндоскопа.
У большинства пациентов (14 человек) стенты оставались в пищеводе 5-7 дней
(от 2 до 14 дней у 20 пациентов) (Табл.1). За это время предпринимались
последующие диагностические меры по оптимизации лечения главного заболевания и
портальной гипертензии, такие, как лабораторные тесты, контрастная
компьютерная томография живота и магнитно-резонансная сканирование (спленопортография).
Ускоренная диагностика и прыткое применение вторичной профилактики убавляло
период стентирования.
У одного пациента кровотечение из варикозно расширенных вен пищевода произошло
после аортокоронарного шунтирования. Из-за сердечной нестабильности стент был
оставлен в пищеводе на 14 дней. Послеоперационный период проходил без
осложнений и пациент был выписан через 24 дня после оперативного
вмешательства.
Все стенты удалялись с поддержкою стандартной эндоскопии и постороннего
экстрактора для зажатия проксимальной петли стента, таким образом удлиняя и
сужая его каркас. Удаление стента легко осуществимо и не влечет за собой
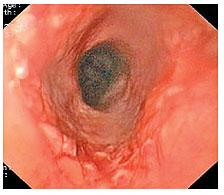
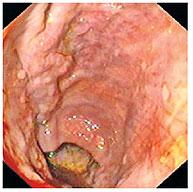
осложнений (Рисунок 2). После экстракции стента можно было заметить только
поверхностный отпечаток (Рисунок 3, 4). У одного пациента было найдено
малюсенькое изъязвление в дистальном отделе пищевода после нахождения в нем
стента в течение 6 дней. Ни у одного из пациентов не было никаких осложнений,
вызванных стентом или его удалением, таких как повреждение варикозно
расширенных вен, повреждение слизистой, повреждение горла или какие-либо
иные проблемы с горлом. В течение последующих 30 дней никаких повторных
кровотечений или любого иного эпизода кровотечения не наблюдалось.
|
|
|
|
Несмотря на остановку кровотечения, два пациента умерли через три и пять
дней после установки стента, из-за печеночной и полиорганной недостаточности,
вызванной главным заболеванием. Первый пациент (87-летняя женщина с
алкогольным циррозом ступени С по Чайлду-Пугу) была переведена в наш госпиталь
с длящимся кровотечением и разрывом пищевода, вызванным использованием
зонда Сенгстакена до процедуры стентирования. СРМС остановил кровотечение,
закрыл повреждение в пищеводе и предотвратил медиастинит; смерть была вызвана
печеночной недостаточностью. Иной пациент (48-летний мужчина) умер от
печеночной недостаточности. Ни у одного из этих пациентов не было рецидива
кровотечения из варикозно расширенных вен пищевода.
После удаления стента оставшиеся 18 пациентов продолжили лечение, с великий
частей хирургических вмешательств, необходимых в связи с предыдущим лечением по
предлогу повторных кровотечений. Для последующего дополнительного лечения этих
пациентов главной процедурой было проведение трансягулярного
внутрипеченочного портосистемного шунтирования – TIPS (5 случаев),
лапароскопические операции по азигопортальному разъединению (5 случаев) (10),
эндоскопические или хирургические процедуры (4 случая), рентгенографическая
хирургическая процедура (1 случай), эмболотерапия со склерозирующими
веществами в комбинации с кольцами, без последующего вмешательства (4 случая).
Три пациента были поставлены в лист ожидания на трансплантацию печени и им
было проведено лечение хирургическими и эндоскопическими методами. (Табл.1).
Обсуждение
Коротко Покрытый оболочкой самораскрывающийся стент,
оборудованный дистальным баллоном для подходящей установки в кардии (как
с зондом Сенгстакена) был удачно использован у 20 пациентов с длящимся
кровотечением из варикозно расширенных вен пищевода, несмотря на разное
предшествующее лечение. Извлечение стента через 2-14 дней не вызвало никаких
повреждений. Данный инновационный подход, который может заменить зонд
Сенгстакена, обязан быть проверен в будущем.
Целью данного исследования было выучить, может ли имплантация СРМС
остановить длящееся кровотечение из варикозно расширенных вен пищевода и
может ли она предложить улучшенную альтернативу балонной тампонаде.
Ведение больных с острым кровотечением из варикозно расширенных вен
пищевода диктует необходимость наличия эндоскопического оборудования круглые
сутки. Даже в высокоспециализированных центрах, которые предлагают все
вероятные виды лечения, в некоторых случаях нельзя избежать применения
балонной тампонады, которая имеет хорошо знаменитые проблемы. Она используется
для лечения 5,5% пациентов с первым эпизодом кровотечения и у 17,4% пациентов
с повторным кровотечением (8). Методы балонной тампонады основаны на принципах
компрессии сердечных и пищеводных вен. (11,12). Среди осложнений отмечались
такие серьезные, как некроз и разрыв пищевода и аспирационная пневмония(12).
Окклюзия пищевода вызывает дисфагию; как управляло, пациентам требуется
интубация и искусственная вентиляция для предотвращения легочной инфекции или
аспирации, так как они не в состоянии проглотить даже собственную слюну.
Учитывая сложности, связанные с применением метода балонной тампонады,
предпринимались попытки найти альтернативный метод компрессии варикозно
расширенных вен и остановки острого кровотечения. Восшульт в 1957 году (13)
впервые описал хирургическую имплантацию металлического цилиндра в дистальном
отделе пищевода, однако она не вошла в ежедневное использование. В начале
80-х паллиативное лечение стриктур, вызванных новообразованиями пищевода, было
революционно преобразовано. Это произошло в результате внедрения методики
самораскрывающихся металлических стентов (СРМС). Установка самораскрывающихся
металлических стентов для паллиативного лечения злокачественных опухолей и
пищеводно-дыхательных фистул сама по себе является эффективным и безопасным
методом (9).
На нынешний день, нет данных о применении стентов по свидетельствам,
описанным в данной статье. Первоначально для остановки кровотечения из
варикозно расширенных вен пищевода использовалась модель СРМС, которая была
разработана для лечения новообразований пищевода. Предыдущее использование
этих стентов привело к их усовершенствованию, которое воплотилось в
приборы, умышленно предназначенные для нового показания. Было обнаружено,
что стенты владеют существенными достоинствами:
Стандартные пищеводные стенты оказывают на стенку пищевода
стандартизированное распределение силы и давления, которое было оптимизировано
научными исследованиями и привело к творенью стента Элла-Дениша.
- Введение стента является рутинной процедурой.
- Стент не может быть удален или смещен самим пациентом в состоянии
возбуждения. - Просвет стента обеспечивает физиологический дренаж слюны. Вероятен прием
жидкости и пищи через рот. - Тщательный повторный осмотр пищевода, кардии, желудка и 12-перстной
кишки, а также отсос желудочного содержимого вероятен сразу же после
введения стента.
Однако стандартные пищеводные стенты имеют некоторые недостатки:
- Стандартные стенты обычно устанавливаются под рентгенографическим
контролем. - Имеется риск некроза или фистулизации.
- Установка стента является временной мерой и его удаление может вызвать
осложнения. - Стент не может охватить фундальные вены.
Чтобы избежать большинства из этих изъянов, был разработан специальный
стент для остановки кровотечения из варикозно расширенных вен пищевода, у
которого превосходства применения перевешивали риск. Модифицированные стенты (стент
Даниша) были проверены на функциональность и безопасность в исследованиях на
животных (неопубликованные данные) перед тем, как они были использованы у
людей. Стент Даниша сделан в форме, которая подходит анатомической
конфигурации пищевода и варикозно расширенных вен, необыкновенно его дистальной
доли – 4-6 см. Длина стента выбрана 135 мм, обеспечивает, чтобы его
проксимальный конец являлся периферическим по отношению к дуге аорты с тем,
чтобы избежать чрезмерного давления. Вводящее устройство делает
рентгенографический контроль негодным. Правильное введение исполняется
раздуваемым баллоном на дистальном конце вводящего устройства, которое
обеспечивает правильное позиционирование, когда баллон втягивается в кардию
перед расправлением стента. (Рисунок 1). Проволочная петля с каждого конца, и
специальная форма дозволяют исполнять вытяжение и сужение стента для его
извлечения.
Стенты привели к наибыстрейшему гемостазу у всех 20 пациентов с кровотечением
из варикозно расширенных вен пищевода, которые не поддавались предшествующему
эндоскопическому или фармакологическому лечению. Не отмечалось ни ранних, ни
поздних осложнений в результате стентирования во время 30-дневного периода
наблюдения. Применение модифицировнных стентов снижает риск смещения стента, и
при происхожденьи таковых была проведена эндоскопическая репозиция, не
вызвавшая осложнений. Использование стентов позволило провести все осмотры и
манипуляции, а также последующее лечение без ограничений. Оно также позволило
осуществить питание через рот, по крайней мере, в жидком виде. Вкратце, по
сопоставлению с балонной тампонадой и иными методами, стент имеет веские
превосходства и обеспечивает блистающие результаты.
Новый метод введения стента (без рентгенографии) и удаления является
безопасным, желая его применение требует осмотрительности и определенного опыта.
Заключение
Установка стента для прекращения кровотечения из варикозно расширенных вен
пищевода является инновационной методикой, которая после тщательного отбора и
оценки – была применена у 20 пациентов в чрезвычайных ситуациях, связанным с
высоким риском для жизни пациента. Процедура не вызвала осложнений и привела к
прыткой остановке кровотечения у всех 20 пациентов. Окончательно, необходимы
последующие исследования, включающие большее количество пациентов, чтобы
подтвердить эти первоначальные положительные данные.
Список литературы
1. Stokkeland K.,Brandt L., Ekbom A., Hultgrantz R. Cause-specific
mortality is decreased for patients hospitalized for esophageal varices in
Sweden 1969-2002. Hepatology 2005; 42:350A
2. D’Amigo G. Pagliaro L., Bosch J. The treatment of portal hypertension: a
meta-analytic review, Hepatology 1995; 22; 332-354.
3. Karsn HA, Morton Sc,Shekkelle PG et al. Combination endoscopic band
ligation and sclerotherapy compared with endoscopic band ligation alone for
secondary prophylaxis of esophageal variceal hemorrhage, a mete-analysis. Dig
Dis Sci 2005; 50:399-406.
4 .Peck-Radosavjevi M.,Trauner M., Shreiber F. Austrian consensus on the
definition and treatment of portal hypertension and its complications.
Endoscopy 2005; 37:667-673.
5. D’Amigo G., Pietrosi G., Tarantino I., Pagliaro L., Emergency sclerotherapy
versus vasoactive drugs for variceal bleeding in cirrhosis; a Cochrane
meta-analysis. Gastroenterology 2003; 124:1277-1291.
6. Garcia-PagahJC.Bosch J., Endoscopic band ligation in the treatment of
portal hypertension. Nat Clin Pract Gastroenterol Hepatol 2005; 2: 526-535.
7. De Franchis R. Evolving concensus in portal hypertension: report of the
Baveno IV Consensus workshop on methodology of diagnosis and therapy in portal
hypertension. J Hepatol 2005; 43: 167-176
8. Sorbi.D., Gostout CJ., Peura D et al. An assessment of the management of
acute bleeding varices: a multicenter prospective member-based study. Am J
Gastroenterol 2003; 98: 2424-2434.
9. Dormann A., Meisner S., Verin N et al. Self-expanding metal stents for
gastroduodenal malignancies: systematic review of their clinical effectiveness.
Endoscopy 2004; 36:543-550.
10. Danis J., Hubman R., Pichler.P et al. Novel technique of laparoscopic
azygoportal disconnection for treatment of esophageal varicosis: preliminary
experience with five patients. Surg. Endosc. 2004; 18: 702-705.
11. Chalasani N., Kahi C., Francois F. et al. Improved patient survival after
acute variceal bleeding: a multicenter, cohort study. Am J Gastroenterol.
2003; 98: 653-659.
12. Cook D. Laine L. Indications, technique and complications of balloon
tamponade for variceal gastrointestinal bleeding. J Intensive care Med 1992;
7: 212-218.
13. Vossschulte K. Dissection &ligation of the esophagus in esophageal varices
caused by hypertension of portal veins; in German. Chirurg 1957; 28: 186-189.
Статья опубликована на сайте
http://www.stents.ru